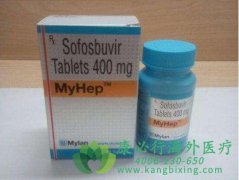
����HCV���Ը�Ⱦ����в���ཡ�����ش����ҹ�Լ��1000������Ⱦ�ߡ�2011��������һЩ���HCV��ֱ�ӿ�����ҩ�DAA�������У������ðе���NS3/4A��NS5A��NS5B,���п�����ЧӦǿ���Ƴ̶̡�������Ӧ�����ʵ͡�����֢�١����÷�Χ�㡢Ӧ�÷��㼰����������...
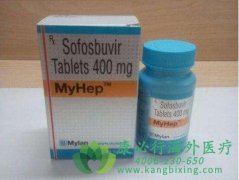
���Dz�Τ �ɼ�����(Gilead)�з�����2013��12��6�ջ�����ʳƷҩƷ������(FDA)�����У� ֮����2014��1��16�ջ��ŷ��ҩ�������(EMA)�����У�������2015��3��26�ջ���ձ�ҽҩƷҽ����е�ۺϻ���(PMDA)�����У��ɼ������������ۣ���Ʒ��ΪSovaldi�� ����...
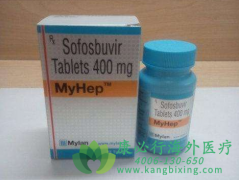
����ֱ�ӿ�����ҩ�DAA�� ���Dz�Τ (SOF)��daclatasvir(DCV)�������ƣ��ܹ���Ч�����������ߵ����Ա����ײ���(HCV)���������ƺ��Ƿ���Ч���Ƹι��ܣ�Ŀǰ���������һ���⡣�����Mohamed�ȿ�չ�о���ּ��̽��ֱ�ӿ�����ҩ�����ƣ��ܷ���Ч���Ƹι���...
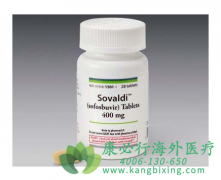
���� ���Dz�Τ Ϊ���������͡������β���ҩ�������Ի���1�ͱ��β������������ã������������͵ı��β�����ȾҲ��Ч�����⣬���Dz�Τ�뵰��ø���Ƽ���ͬ���������������ײ�����ҩ�ԣ���ʹ��������ҩ�ԣ�ͣҩ����ҩ�����ܿ���ʧ�����Ը�����һ��ҩ�����ϣ��ٴ�...
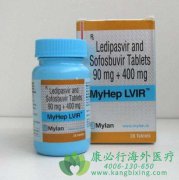
���Dz�Τ ������Ϊ������Τ��Ӣ����Sofosbuvir,��Ʒ��Sovaldi���Ǽ����¹�˾���������������Ա��ε���ҩ�����Dz�Τ������ʳƷҩƷ�ල�����֣�FDA������2013��12��6�����������У���ֱ�������ŷ�������й�������������Ϊ���Ͽ��������Ʒ����е���ϳɷ�...
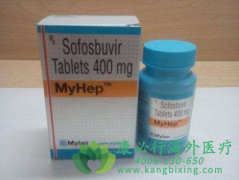
���Dz�Τ ��л����ΪGS-331007��Ϊ�����ײ�����HCV��������NS5B�ۺ�ø�ĺ������Ƽ��������ðе���HCV������NS5B�ۺ�ø�߶ȱ��صĻλ�㡣������������������ϸ�������ữ���Ϊ�л��Ե���������գ�����HCVRNA�������õĺ��վ������Ӷ�ʹHCV�����鸴����...
�����ڵ�26����̫�����о�ѧ����ᣨAPASL���Ϲ����� ���Dz�Τ �����й�����1��2��3��6�����Ա��λ��ߵ�III���ٴ��о����ݡ�����ű�ǩ��III���о����й�26��ҽԺ��ļ��389�����д����Ը�Ӳ������Ӳ���ı������ߣ��������ǵĻ����ͺ����������ԣ�...
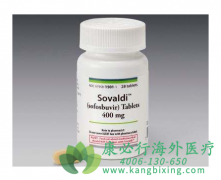
���Dz�Τ ��������Pharmasset��˾��Michael Sofia��ʿ�Ŷ����������ģ���Gilead��2011����110����Ԫ�չ�����Ϊȫ�����������ڱ��Ͳ����Ը���ȫ�ڷ����Ʒ���ҩ�2013��12��6�վ�����FDA�����������У�2014��1��16�վ�ŷ��ҩƷ������ (EMEA) ����...
����III���о����й�26��ҽԺ��ļ��389�����д����Ը�Ӳ������Ӳ���ı������ߣ��������ǵĻ����ͺ����������ԣ������� ���Dz�Τ ������Τ�֣�RBV������/���Ҷ��������أ�PegIFN�������£������й�����1��2��3��6�����Ա��λ��ߵ�Ч�����������Ʒ�...
��������һֱ�����dz�Ϊ����Ĭ��ɱ�֡�����ȫ�������������ŵ�ʮλ������Ŀǰ��ͳ�ƽ����ʾ�ˣ�ȫ����λ���1.7�ڣ����ҹ��ı��θ�Ⱦ�߾�����ǧ���������ײ�ͬ���ǣ��������Ը�Ⱦ�����Ƚ��ᣬ���Ǹ�����չ�����ԣ�Ҳ��������Ӳ�����������ʺ�...
�����ѯ�绰��4006 130 650


