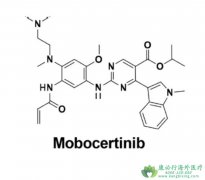
2021年9月15日,美国食品药物管理局(FDA)批准了武田制药的 Mobocertinib 上市申请,适应症为用于治疗在含铂化疗治疗期间或治疗后进展的局部晚期或转移性的EGFR 20ins患者。 Mobocertinib 是武田研发的一种新型、高选择性、靶向 EGFR 20ins的口服酪氨酸...
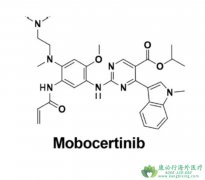
Mobocertinib (TAK-788,商品名EXKIVITY)是武田(Takeda)制药的一款口服EGFR酪氨酸激酶抑制剂。2021年9月15日,美国FDA加速批准上市,用于治疗在含铂化疗治疗期间或治疗后进展的局部晚期或转移性的,EGFR外显子20插入突变阳性的非小细胞肺癌(NSCLC...
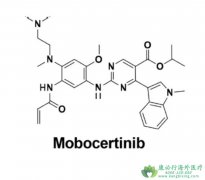
EGFR ex20ins突变是NSCLC患者常见EGFR突变类型之一,既往一段时间内未取得突破性治疗进展。随着研究的不断深入,靶向突变NSCLC的治疗药物层出不穷,多款新药进入临床研究,以Amivantamab、 Mobocertinib (TAK-788)为代表的新疗法率先崭露头角,获FDA批...
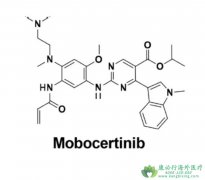
2021年9月15日,美国FDA加速批准 Mobocertinib 上市,用于治疗含铂化疗期间或之后疾病进展的EGFR exon20 ins局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。Exkivity获得FDA优先审理,并获得突破性疗法认定、快速通道审评资格认定和孤儿药资格认定,是首...
美国NDA于2021年4月获得FDA授予优先审评资格,此次在中国的上市许可申请获得受理首次实现了中国与全球的同步递交,将助力加速武田创新药早日惠及中国患者。EGFR 20号外显子插入突变是非小细胞肺癌(NSCLC)中的一种罕见突变,在中国,号外显子插入突变发...
EGFR 20外显子插入突变(20ins)属于EGFR少见突变,发生率远低于19外显子缺失突变和21外显子L858R突变,现有EGFR-TKI的疗效不尽人意,亟需更好的治疗选择。由于中国肺癌患者EGFR突变率较高,因此EGFR 20ins突变患者的数量不容忽视,他们的治疗研究进展更值得...
1/2期试验评估了口服 Mobocertinib 治疗非小细胞肺癌(NSCLC)的安全性、药代动力学和抗肿瘤活性。该试验包括1期剂量递增试验,评估Mobocertinib作为单一疗法和联合化疗,几个扩展队列和表皮生长因子受体(EGFR)外显子20插入突变阳性转移性NSCLC(mNSCLC)患...
EGFR ex20ins突变是常见的EGFR突变类型之一,具有高异质性,由于既往缺乏有效的靶向治疗药物,只能接受EGFR TKI、化疗、免疫治疗,但临床获益有限,亟需新疗法。 Mobocertinib (TAK-788)作为FDA批准的首款专门为携带EGFR ex20ins突变NSCLC患者设计的口服疗...
2021年9月15日,根据日本武田制药(Takeda)公司最新披露的消息,该公司研发的肺癌新药EXKIVITY已获美国食品药品监督管理局(FDA)加速批准上市,用于治疗接受以铂为基础的化疗期间或之后疾病进展的EGFR 20外显子插入(ex20ins)突变的局部晚期或转移性非小...
2021年9月15日,肺癌创新产品 Mobocertinib (EXKIVITY)获得美国食品药物管理局(FDA)批准,Mobocertinib(TAK-788,商品名EXKIVITY)是武田(Takeda)制药的一款口服EGFR酪氨酸激酶抑制剂。适应症为用于治疗在含铂化疗治疗期间或治疗后进展的局部晚期...
免费咨询电话:4006 130 650


