
今日,第一三共(Daiichi Sankyo)公司宣布,日本厚生劳动省(MHLW)批准该公司开发的口服FLT3抑制剂 Vanflyta (quizartinib)上市,治疗复发/难治性(R/R) 急性骨髓性白血病 (AML)患者。这些患者携带FLT3-ITD基因变异。AML是一种进展迅速的血液和骨...
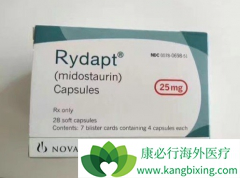
雷德帕斯(Rydapt)是首个与化疗疗法联合用于治疗 急性髓性白血病 (AML)的靶向药物,但是用药过程中,也会出现副作用。RYDAPT在AML患者中最常见的副作用包括:低白细胞计数伴发热(发热性中性粒细胞减少症);恶心;口腔内发红,疼痛或溃疡(粘膜炎);呕...

Cusatuzumab 是杨森公司从argenx公司获得的创新抗CD70单克隆抗体。CD70是血液癌症,部分实体瘤,以及自身免疫疾病中的一种免疫检查点蛋白。Cusatuzumab能够通过与CD70结合产生多种抗癌作用,包括通过补体依赖性细胞毒性杀死表达CD70的癌细胞,激发肿瘤...
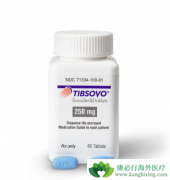
今日,Agios Pharmaceuticals公司宣布,美国FDA批准该公司开发的IDH1抑制剂 Tibsovo 扩展适应症范围,用于一线治疗携带易感异柠檬酸脱氢酶-1(IDH1)基因突变的 急性骨髓性白血病 (AML)患者。这些患者超过75岁或者由于其它合并症不能接受强力诱导化疗...
FLT3阳性的 急性骨髓性白血病 是白血病的一种,多见于成人,并随年龄的增长而发病率随着增加。对常规的化疗治疗响应率不佳,并且容易复发,五年的生存率很低。近二十多年来,对于白血病治疗方面并无很大的突破,直到雷德帕斯的获批上市,才打破了这个局...
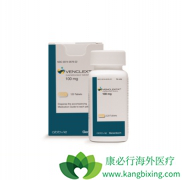
11月21日,FDA加速批准venetoclax( Venclexta )联合阿扎胞苷/地西他滨,或低剂量阿糖胞苷,治疗新确诊的75岁及以上的AML患者,这些患者因为自身健康问题无法使用高强度化疗。 此次批准是基于两项临床试验,M14-358 (NCT02203773)和M14-387 (NCT022...

FDA方面也表示,Kymriah的剂量是根据使用的患者自身T细胞所产生的定制治疗。患者的T细胞被收集并送到制造中心,在进行遗传修饰以包括含有特异性蛋白质(嵌合抗原受体或CAR)的新基因,其指导T细胞靶向并杀死具有表面上的特异性抗原(CD19)。一旦细胞被修饰,它们被注入到患...
今天,美国FDA批准了Daurismo与低剂量阿糖胞苷(LDAC)联合使用治疗 急性骨髓性白血病 (AML)。LDAC是一种化疗,用于治疗75岁成人新诊断的AML。临床试验显示,使用Daurismo联合LDAC可以提高整体存活率,而不能耐受强化疗的患者只能使用LDAC。AML是一种...
今日,艾伯维(AbbVie)和罗氏(Roche)旗下基因泰克(Genentech)公司共同宣布,FDA加速批准双方共同开发的 Venclexta (venetoclax),与低甲基化剂(azacitidine或decitabine),或低剂量阿糖胞苷(LDAC)化疗联用,治疗新确诊75岁以上,或因为慢性健...
美国当地时间2018年7月20日,Agios Pharmaceuticals,Inc.宣布FDA批准了该公司研发的用于治疗复发性或难治性急性髓性白血病(R/R AML)的创新药TIBSOVO (ivosidenib)。 TIBSOVO 是靶向异柠檬酸脱氢酶1(isocitratedehydrogenase1,IDH1)的小分子口服...
免费咨询电话:4006 130 650


