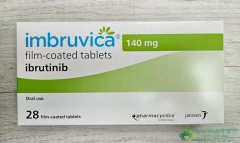
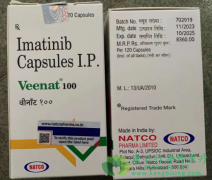
2018年9月24日,安斯泰来制药公司总裁兼首席执行官Kenki Yasukawa博士宣布,欧洲药品管理局人用药委员会(CHMP)采取了将Xtandi(恩杂鲁胺)的适应症扩大到包括具有高风险非转移性去势抵抗性前列腺癌(nmCRPC)的成年男性的积极意见,如果该提议得到欧盟委员会(EC)的批准 ,恩杂鲁胺将是用于这一疾病关键阶段的首批治疗方法之一,同时也扩大了该药的用药群体。
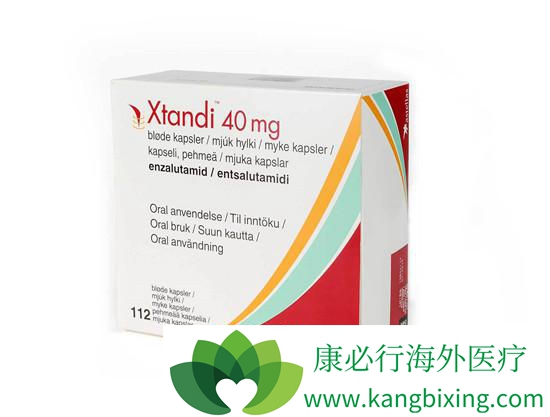
恩杂鲁胺其临床药物是由Medivation 公司和安斯泰来( Astellas) 公司合作开发,于2012年8 月31 日经美国食品药品管理局( FDA) 批准用于治疗已扩散或复发的晚期男性去势耐受前列腺癌(CRPC) ,商品名为Xtandi,该药为口服制剂,2018年7月13日,FDA批准该药物用于非转移性CRPC(NM-CRPC)患者,扩大了用药的群体。恩杂鲁胺于2013年6月首次获得EC批准,用于疾病已恶化或雄激素剥夺治疗(ADT)失败后无症状或轻度症状或以多西他赛治疗后的 mCRPC 患者。
CHMP的观点是基于关键的3期PROSPER试验的结果,这项研究一共招募了1401名患者,该试验评估了恩杂鲁胺加ADT与安慰剂加ADT对nmCRPC患者和前列腺特异性抗原(PSA)水平快速上升的影响, 试验结果表明,恩杂鲁胺与ADT构成的组合疗法与ADT与安慰剂组合疗法相比显着延长患者的无转移生存期 (MFS) ,该结果符合无转移生存(MFS)的主要终点。接受恩杂鲁胺加ADT的男性中位MFS为36.6个月,而安慰剂加ADT的患者为14.7个月(n = 1401; HR = 0.29 [95%CI:0.24-0.35]; p <0.001)。
详情请访问 肿瘤 http://www.kangbixing.com/



 添加康必行顾问,想问就问
添加康必行顾问,想问就问