2018年10月16日,Talzenna(Talazoparib)获得美国FDA批准上市,用于治疗携带胚系BRCA突变(有害或疑似有害),HER2阴性的局部晚期或转移性乳腺癌患者。Talazoparib是辉瑞公司研发的新一代PARP抑制剂,临床前研究显示,Talazoparib有较强的催化阻滞活性和PARP捕获潜力,相比于目前在研的其他PARP抑制剂,抑制PARP蛋白的活性强100倍。本次获批是基于III期EMBRACA研究,比较了Talazoparib和临床医生选择的标准化疗治疗携带BRCA1/2胚系突变的局部晚期或转移性乳腺癌的疗效和安全性。
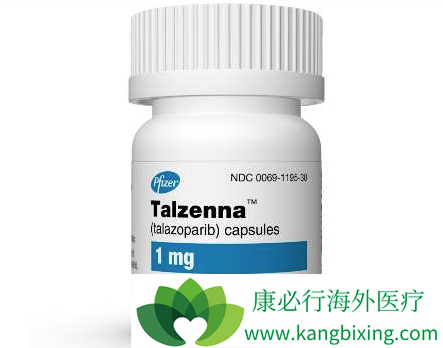
EMBRACA是一项随机,开放标签的3期临床试验,该研究在全球16个国家145个研究中心招募了431例携带胚系BRCA1/2突变,患有局部晚期或转移三阴性(TNBC)或激素受体阳性(HR+)/HER2-的晚期乳腺癌患者。所有患者需要携带有害或疑似有害的胚系BRCA突变;对于局部晚期或转移性疾病,必须接受不超过3次的细胞毒性化疗方案;在新辅助治疗,辅助治疗和/或转移治疗中,患者需要接受蒽环类和/或紫杉烷治疗(除非是禁忌)。排除在接受晚期乳腺癌的铂类化疗时具有客观疾病进展的患者(即,根据实体肿瘤的反应评价标准[RECIST]1.1版,在最后一次给药后约8周内,患者不能患有进行性疾病)。激素受体阳性(HR+)乳腺癌患者接受的激素治疗数量不受限制。已完成明确的局部治疗,在重复脑成像时CNS病变稳定,并且接受低剂量或无糖皮质激素治疗的患有中枢神经系统(CNS)转移的患者符合条件。
试验结果表明,与标准化疗组相比,Talazoparib治疗组的中位无进展生存期显著延长(8.6个月 vs 5.6个月,p<0.001),并且PFS获益在所有临床相关亚组中一致。Talazoparib治疗组疾病进展或死亡风险显著降低46%。
更多新闻请您访问 肿瘤 http://www.kangbixing.com/



 添加康必行顾问,想问就问
添加康必行顾问,想问就问