��������������2015�걻FDA�������������ڣ�ת���ԣ����ٰ�������һ����ø���Ƽ�����������������Ϊ�дƼ�������(ER)-���ԣ��˱�Ƥ������������2(HER2)-���������鰩������Ů��������Ϊ��ʼ�����ڷ������ƶ���ת�Ƽ����������Ӧ֤�Ǹ�����չ����(PFS)�ڼ������±���������������Ӧ֤����ȡ��������֤���������ٴ������֤����������
����
����1����Ӧ֤����;��IBRANCE�����������������ö��дƼ�������(ER)-���ԣ��˱�Ƥ������������2(HER2)-���������鰩������Ů��Ϊ��ʼ�����ڷ������ƶ���ת�Ƽ��������ơ������Ӧ֤�Ǹ�����չ����(PFS)�ڼ������±�����[���ٴ��о�(14)]���Դ���Ӧ֤�ļ���������ȡ��������֤���������ٴ������֤����������
����
����2��������ҩ������
����
����2.1 һ���ҩ��Ϣ��IBRANCE���Ƽ�������һ��125 mg���ҿڷ�����ÿ��һ�ι�21��������Ų�������7�����һ��28�������Ƴ̡�IBRANCEӦ��ʳ�����[���ٴ�ҩ��ѧ(12.3)]��������2.5 mgÿ��һ����������28-���Ƴ���ʼ���ո��衣Ӧ����������ÿ��ӽ���ͬʱ��������ǵļ������综��Ż�»�ʧһ���������첻Ӧ���������������Ѱ����ʱ�������һ�δ���������IBRANCE����Ӧ������(������ǰ��Ҫ����ѹ������)�������飬ѹ�������ʱ��Ӧ���뽺�ҡ�
����
����2.2 ����������������ݸ��尲ȫ�Ժ������Ե���IBRANCE����[�������ע������(5)]��
����
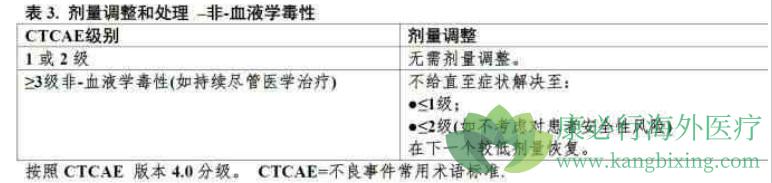
����ijЩ������Ӧ�Ĵ���[�������ע������(5)]������Ҫ��ʱ�жϼ���/�ӳٺ�/����ͼ�������������ֹ��ͬ��1��2��3�ṩÿ�ּ������ͼƻ�[�������ע������(5)��������Ӧ(6)���ٴ��о�(14)]������
�����������̴������϶Թ�ͬ��ҩ��Ʒ���������ڶ����¼��м�������ָ��ԭ���������ذ�ȫ�����ϻ����֤��
����
����Ϊ��ǿCYP3A���Ƽ�ʹ�ü���������
����
��������ǿCYP3A���Ƽ���ͬʱʹ�úͿ���û�л�СCYP3A������������ͬʱҩ��综�߱�����ǿCYP3A���Ƽ���ͬ��ҩ������IBRANC������75 mgÿ��һ�Ρ���ǿ���Ƽ�����ֹ������IBRANCE����(���Ƽ���3�C5����˥�ں�)��ǿCYP3A���Ƽ�ʹ��ǰ����[��ҩ�������(7.1)���ٴ�ҩ��ѧ(12.3)]��
����
����3�����ͺ��125 mg���ң�����Ӳ�������ң���С0���н���ñ���壬ñ���ð�ī֭ӡ�����ϡ�PBC 125����100 mg���ң�����Ӳ�������ң���С1���н���ñ��dz��ɫ�壬ñ���ð�ī֭ӡ�����ϡ�PBC 100����75 mg���ң�����Ӳ�������ң���С2����dz��ɫñ���壬ñ���ð�ī֭ӡ�����ϡ�PBC 75����
����
����4������֤ ��
����
������������� �������� https://www.kangbixing.com





 ���ӿ����й��ʣ����ʾ���
���ӿ����й��ʣ����ʾ���