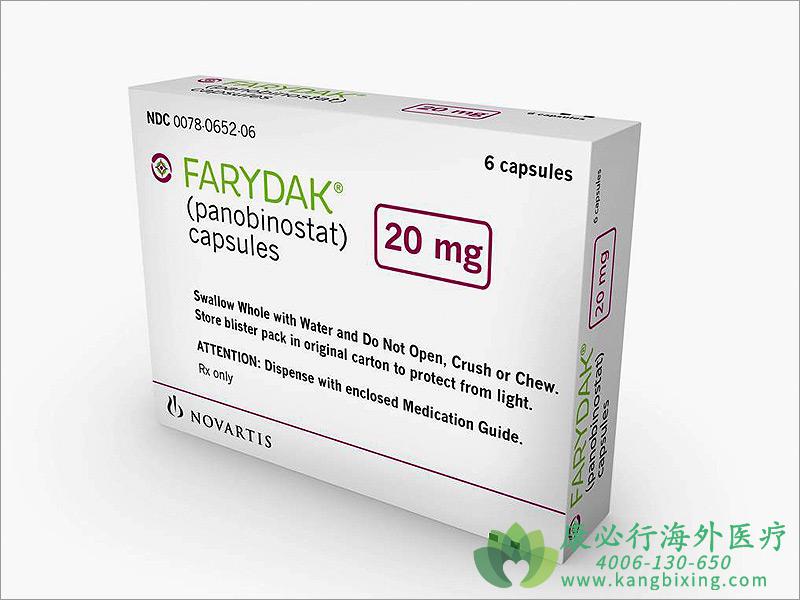
��������˾��Farydak(��obinostat������LBH589)�������������͵�����������ʹ���ѻ�����ʳƷ��ҩ�������(FDA)�������������ѽ�������������ǰ�Ʒ��Ķ�Թ��������ߣ����������������ߵ��ڼ�(IMiD)��
��������˾�������FDA�ļ���������Ϊ��֤���˸û���Ⱥ������������Ʒ�����չ������(PFS)���ơ���ŵ����˾�ƣ�Farydak�������ڶ�Թ��������ߵ��鵰����������ø(HDAC)���Ƽ���
������Թ����������ٴ��о����μ��о���Ա���ޡ�����ɭ˵������Ҫ���ǣ���֤������˾�����Ը��ƶ�Թ������������ߵ���չ�����ʣ���Щ�������ٽ������������Ʒ�����������������IMiD,����ҽ������δ�õ����������
������������Ч�Ͱ�ȫ�����ݣ����о�����Ԥ��ָ�����������������III�������˫ä����ο�����գ�������ȫ��ע�������ڼ���ܹ���������IMiD�������Ƶ�193�����߽�����ȫ������-1(��Թ������е�PANobinostat ORA1)��
�����о��������밲ο������ȣ����ܹ���������IMiD˫�����Ƶ�Farydak���ߵ�PFS������λ�����ӡ�Farydak�����˶�Թ���������ҩ���Ϊ��Щ�����ṩ����������������֢����Ҫ���Ʒ�����������Ҫ������ѯ�����к���ҽ��ҽѧ���ʣ�4006-130-650��ɨ�������·��ţ����ǽ��߳�Ϊ������
��������ҩƷ��������� ����˾�� https://www.kangbixing.com/drug/pabisita/



 ���ӿ����й��ʣ����ʾ���
���ӿ����й��ʣ����ʾ���