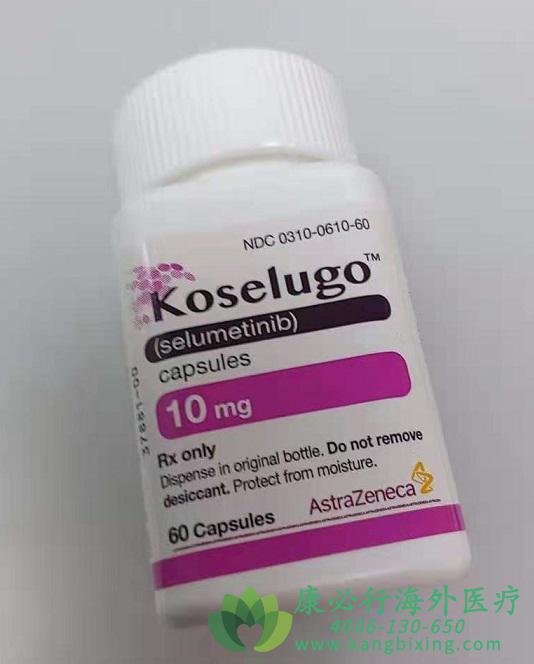
神经纤维瘤1型的儿童患者有了新药。这个刚刚获得欧盟有条件批准的新药是司美替尼,司美替尼用于治疗用于治疗3岁及以上的1型神经纤维瘤病(NF1)儿童患者的症状性、无法手术的丛状神经纤维瘤(PN)。
神经纤维瘤1型(NF1)是一种使人衰弱的遗传病,全世界每3,000人中就有一人受到影响。在30-50%的NF1患者中,因为肿瘤在神经鞘上发展(丛状神经纤维瘤),可能导致毁容又疼痛的各种临床问题,如:毁容、运动功能障碍、疼痛、气道功能障碍、视力障碍和膀胱或肠道功能障碍。
这个批准是根据一个试验,Sprint二期临床试验,结果表明,司美替尼(上市名:Koselugo)减少了无法手术治疗的NF1型儿童的肿瘤的大小,减轻了疼痛,并提高了生活质量。司美替尼是欧盟首次批准的治疗NF1丛状神经纤维瘤(NF1-PN)的药物,这个批准是在2021年4月的人用药品委员会(CHMP)的积极建议后做出的。司美替尼由阿斯利康(AstraZeneca)和默沙东(MSD)合作。欧盟批准意味着司美替尼在28个成员国允许上市。司美替尼是丝裂原活化蛋白激酶激酶1和2(MEK1/2)的抑制剂。
MEK1/2蛋白是细胞外信号相关激酶(ERK)通路的上游调节剂。该通路通常在不同类型的癌症中被激活。司美替尼于2019年4月获得美国FDA突破性疗法指定,2019年12月获得罕见儿科疾病指定,并于2018年2月获得美国孤儿药指定。欧盟、日本、俄罗斯、瑞士、韩国、台湾和澳大利亚已授予孤儿药指定。Sprint二期试验是由美国国立卫生研究院国家癌症研究所(NCI)癌症治疗评估计划(CTEP)赞助。作为罕见病用药,这个有条件批准让新药更快获批上市。批准的条件是更长的随访时间的试验的安全性和有效性数据。
“对于1型神经纤维瘤病患儿,丛状神经纤维瘤可以显着生长和发展,”SPRINT试验首席研究员兼国家肿瘤中心的小儿肿瘤科主任BrigitteC.Widemann医学博士说。“在SPRINT试验中,司美替尼在66%的患者中缩小了NF1相关PN,并且在从状神经纤维瘤相关症状方面显示出具有临床意义的改善。”如有需要,请咨询康必行海外医疗医学顾问:4006-130-650或扫码添加下方微信,我们将竭诚为您服务!点击拓展阅读:司美替尼(SELUMETINIB)是什么药?可以治疗什么病症患者?



 添加康必行顾问,想问就问
添加康必行顾问,想问就问