Scemblix (Asciminib)由诺华公司研发,FDA批准用于治疗慢性髓系白血病(CML)的2种不同适应症:Scemblix治疗处于慢性阶段的费城(Ph)染色体阳性CML患者,此前接受过两种以上酪氨酸激酶抑制剂(TKI)的治疗;治疗携带T315I突变的上述患者。 Scem...
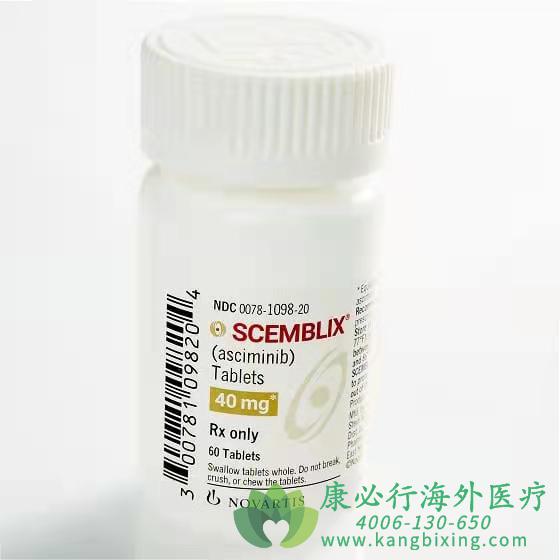
美国食品药品监督管理局FDA批准STAMP抑制剂Scemblix(asciminib)上市,用于治疗慢性髓系白血病(CML)的2种不同适应症:先前已接受过至少2种酪氨酸激酶抑制剂(TKI)治疗、费城染色体阳性慢性髓性白血病慢性期(Ph+CML-CP)成人患者;携带T315...
在2020年美国血液学会(ASH)年会12月8日进行的全体科学会议上,一项全球多中心3期随机对照研究――ASCEMBL研究入选LBA口头报告研究,备受瞩目,这项研究旨在比较口服 asciminib 与bosutinib对既往应用≥2个酪氨酸激酶抑制剂(TKIs)治疗的慢性粒细胞性...
FDA加速批准 asciminib (Scemblix)用于治疗费城染色体(Ph)阳性慢性髓系白血病(CML)的慢性期患者,这些患者既往接受过至少2种酪氨酸激酶抑制剂(TKIs)的治疗。此外,该药还获得了完全批准,用于ph阳性、携带T315I突变的慢性期CML患者。慢性髓系白血病(CML...
诺华公司宣布欧盟委员会 (EC) 已批准 Scemblix (asciminib) 用于治疗先前与两种或多种酪氨酸激酶抑制剂 (TKI) 治疗的费城染色体阳性慢性期慢性髓细胞白血病 (Ph+ CML-CP) 成年患者。此次批准,Scemblix成为欧洲第一款通过专门靶向ABL肉豆蔻酰口袋的CML疗法(...
2021年10月29日诺华(Novartis)公司宣布,美国食品药品监督管理局FDA批准STAMP抑制剂 Scemblix (asciminib)上市,用于治疗慢性髓系白血病(CML)的2种不同适应症:先前已接受过至少2种酪氨酸激酶抑制剂(TKI)治疗、费城染色体阳性慢性髓性白血病慢性...
Scemblix 是一种激酶抑制剂,于2021年10月获得美国FDA加速批准,用于治疗先前已接受过至少2种TKI治疗的Ph+CML-CP成人患者。Scemblix是一款STAMP抑制剂,是一款通过特异性靶向BCR-ABL1蛋白肉豆蔻酰口袋(STAMP)发挥作用的CML治疗药物。目前已上市的竞争...
2022年6月24日,诺华宣布获得CHMP积极意见反馈,其建议相关部门授予 Scemblix (asciminib)上市许可,适应症为处于费城染色体阳性的慢性髓细胞细胞白血病(Ph+ CML-CP)慢性期的成人患者,且患者此前已接受过两种或多种酪氨酸激酶抑制剂(TKI)的治疗。 ...
大多数慢粒患者都会对初始酪氨酸激酶抑制剂治疗产生反应,并在疾病进展后换用另一种酪氨酸激酶抑制剂。 在序贯治疗中,可能会发生由ABL激酶区的点突变驱动的耐药性,特别是“守门人”T315I突变,这是一个临床难题。Ponatinib是仅有的能够战胜T315I突...
2022年08月29日,诺华公司宣布欧盟委员会 (EC) 已批准 Scemblix (asciminib) 用于治疗先前与两种或多种酪氨酸激酶抑制剂 (TKI) 治疗的费城染色体阳性慢性期慢性髓细胞白血病 (Ph+ CML-CP) 成年患者。 此次批准,Scemblix成为欧洲第一款通过专门靶向ABL肉...
免费咨询电话:4006 130 650


