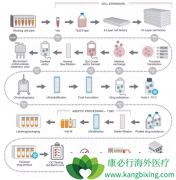
对于 CAR-T 细胞疗法来说,2017年是具有里程碑意义的年份。2017年8月31日,FDA批准首个CAR-T疗法Kymriah上市,诺华为其定价47.5万美元;2017年10月19日,FDA批准第二款CAR-T疗法Yescarta上市,Kite Pharma为其定价37.3万美元。 CAR-T疗法不同于...
经过基因工程改造的T细胞被称为 CAR-T 细胞(chimeric antigen receptor T cell,嵌合抗原受体T细胞)。过去几年,已经有数十项研究对这种免疫细胞进行了测试,将近1000名晚期白血病或淋巴瘤患者参与了临床试验。在此过程中,一半甚至更多患者的寿命超过...

Kymriah 是一款基于基因改造的自体T细胞免疫疗法。该疗法在提取患者的T细胞后,通过基因改造,将一种特定的蛋白(嵌合抗原受体,即CAR)装入T细胞。经过改造的T细胞重新注射入人体后,能够特异性识别白血病细胞表面的抗原(CD19),并将其杀死。 ...
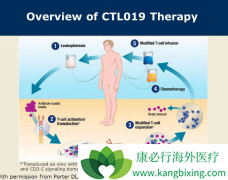
FDA 肿瘤药物咨询委员会(ODAC)以 10:0 的全票通过表决结果,一致建议批准一种治疗癌症的「新药物」上市。这种「药物」是一种代号为 CTL019 的细胞,它是一种名为「 CAR-T 」的疗法中最有代表性的一个。CTL019 这种细胞「药物」,适用人群是罹患急性淋...

近日,美国医保CMS(美国医疗保险和医疗补助服务中心)疯狂宣布,同意为高昂的 CAR-T 疗法费用买单,将向医院支付数十万美元,用于CAR-T疗法治疗特定的癌症患者。具体而言,CMS会为接受吉利德CAR-T治疗的患者支付40万美元,为接受诺华CAR-T治疗的患者支...
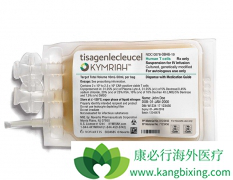
诺华和Kite制药的 CAR-T 药物Kymriah、Yescarta先后被美国FDA批准上市,分别用于治疗25岁以下复发难治性B细胞白急性淋巴细胞白血病和复发难治性大B 细胞淋巴瘤,开启了细胞治疗波澜壮阔的时代。虽然CAR-T细胞技术在血液肿瘤治疗方面获得了公认的较好疗效...

CAR-T 全称是Chimeric Antigen Receptor T-Cell Immunotherapy,嵌合抗原受体T细胞免疫疗法,它的基本原理就是利用病人自身的免疫细胞来清除癌细胞。1989年以色列科学家研发出第一代CAR-T ,然而很可惜,它在临床上并没有什么疗效。直到2010年,CAR-T...

2017年8月31日,FDA发布了批准CD19-CART细胞药物上市的重磅消息,这也是FDA批准的第一个 CAR-T 药物,CD19-CART的适应症是急性淋巴细胞性白血病的儿童和年轻患者,该药成功获批,不仅是诺华的胜利,更是全球CAR-T细胞疗法研究人员的重大成果,为所有癌症...
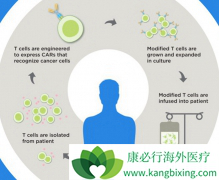
2017年是CAR-T疗法的元年,FDA批准了两款 CAR-T 疗法上市。第一款是来自诺华的Kymriah,于2017年8月获批。用于治疗复发或难治性(R/ R)B细胞急性淋巴细胞白血病(ALL)的儿童和年轻成人(25岁以下)患者。第二款CAR-T细胞疗法Yescarta于2017年10月获得FDA批准...
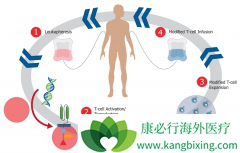
肿瘤免疫疗法是当前研发热点之一, CAR-T 是一项具有划时代意义的突破技术。2011年,美国宾夕法尼亚大学Carl H. June 教授团队的CAR-T 疗法在1例慢性淋巴细胞白血病(CLL)患者治疗的中获得突破,2012年,June团队使用CAR-T治疗急性淋巴细胞性白血病(ALL)7...
免费咨询电话:4006 130 650


