2025年8月,美国食品药品监督管理局(FDA)加速批准了多达维普龙(Modeyso/dordaviprone/ONC201),用于治疗年龄至少1岁、携带H3K27M突变且在先前治疗后出现疾病进展的成人和儿童弥漫性胶质瘤患者。它可是一种蛋白酶激活剂,还是首个获FDA批准用于治疗H3K27M突变型弥漫性中线胶质瘤的全身疗法。这就像是找到了一把新的钥匙,有望打开攻克这类疾病的大门。
获批依据:5项开放标签试验提供关键数据支撑
多达维普龙获批的背后,是美国开展的5项开放标签试验。这些试验严格依据《神经肿瘤学高级别胶质瘤疗效评估标准》(RANO-HGG),对多达维普龙单药治疗携带H3 K27M突变、病情进展且可评估的弥漫性中线胶质瘤患者的疗效进行了全面评估。
这5项研究分别是ONC006试验(NCT02525692)、ONC013试验(NCT03295396)、ONC014试验(NCT03416530)、ONC016试验(NCT05392374)和ONC018试验(NCT03134131)。它们从不同角度对多达维普龙的疗效进行了考察,确保了数据的全面性和可靠性。通过这些试验,研究人员能够深入了解药物在实际治疗中的效果,为FDA的审批提供了坚实的基础。
疗效显著:总缓解率及缓解持续时间数据可观
在由50名可评估的成年和儿童患者组成的综合疗效人群中,多达维普龙展现出了一定的治疗效果。其总缓解率(ORR)为22%(95%置信区间为12%-36%)。这意味着在接受治疗的患者中,有相当一部分人的病情得到了不同程度的缓解。
此外,缓解持续时间中位数(DOR)为10.3个月(95%置信区间为7.3-15.2个月)。在有缓解的患者中,分别有73%和27%的患者缓解持续至少6个月和12个月。这些数据表明,多达维普龙不仅能够使患者病情得到缓解,而且缓解效果具有一定的持久性,能够在较长时间内改善患者的病情,提高患者的生活质量。
多达维普龙(Modeyso/dordaviprone/ONC201)说明书介绍
【适应症】Modeyso(dordaviprone)适用于治疗1岁及以上年龄、患有携带H3 K27M突变的弥漫性中线胶质瘤且在接受先前治疗后病情进展的成人和儿童患者。该适应症已根据缓解率和缓解持续时间获得加速审批。持续审批可能取决于确证性试验中对临床益处的进一步验证和描述。
【作用机制】Dordaviprone是线粒体酪蛋白水解蛋白酶P(ClpP)的蛋白酶激活剂,同时具有多巴胺D2受体抑制作用。在携带H3 K27M突变的弥漫性中线胶质瘤中,该药物通过激活综合应激反应、诱导细胞凋亡及恢复组蛋白H3 K27三甲基化,发挥抗肿瘤活性。体外及体内模型证实其对H3 K27M突变胶质瘤具有显著疗效。
【药品规格】125mg*10粒
【副作用】
最常见(≥20%)不良反应包括疲劳、头痛、呕吐、恶心及肌肉骨骼疼痛。
最常见(≥2%)3级或4级实验室异常为淋巴细胞减少、血钙降低及丙氨酸氨基转移酶升高。
【用法用量】
患者选择:根据肿瘤样本中H3 K27M突变检测结果选择适合接受Modeyso治疗的患者。
监测要求:在开始治疗前及治疗期间根据临床指征定期监测心电图和电解质水平。
成人推荐剂量:每周口服625毫克。
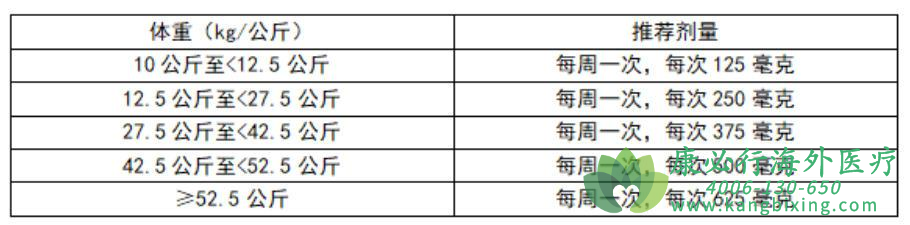
儿童推荐剂量:体重≥10公斤的儿科患者需基于体重调整剂量(见表1)。
表1:儿科患者基于体重的推荐剂量
表1
给药方式:每周空腹口服一次(至少在进食前1小时或进食后3小时)。
治疗持续时间:持续用药直至疾病进展或出现不可接受的毒性。
【注意事项】
超敏反应
若发生具有临床意义的超敏反应或过敏反应,应立即停用Dordaviprone,并启动适当的医疗治疗和支持性护理。
QTc间期延长
Dordaviprone会导致浓度依赖性的QTc间期延长。对于出现QT间期延长的患者,应暂停或减少Dordaviprone的剂量;对于出现危及生命的心律失常迹象的患者,应永久停用Dordaviprone。
胚胎-胎儿毒性
可能对胎儿造成伤害。建议患者了解对胎儿的潜在风险,并采取有效的避孕措施。
【特殊人群用药】
妊娠期
孕妇使用Dordaviprone可能会对胎儿造成伤害。目前尚无孕妇使用Dordaviprone的相关数据来评估药物相关风险。应告知孕妇本品对胎儿的潜在风险。
哺乳期
目前尚无关于Dordaviprone或其代谢物在人乳中存在情况、对母乳喂养婴儿的影响或对乳汁生成影响的数据。由于Dordaviprone可能对母乳喂养的婴儿造成严重不良反应,建议女性在接受Dordaviprone治疗期间及最后一剂后1周内不要进行母乳喂养。
有生殖潜力的女性和男性
建议有生殖潜力的女性在接受Dordaviprone治疗期间及最后一剂后1个月内采取有效的避孕措施;建议有生殖潜力的男性患者在接受Dordaviprone治疗期间及最后一剂后1个月内采取有效的避孕措施。基于Dordaviprone的作用机制(多巴胺D2受体抑制和线粒体功能改变),使用Dordaviprone治疗可能会对男性和女性的生育力产生不利影响。
儿科用药
Dordaviprone在1岁及以上儿童患者中治疗携带H3K27M突变的弥漫性中线胶质瘤的安全性和有效性已得到证实。在1岁以下儿科患者中的安全性和有效性尚未确立。
老年患者用药
Dordaviprone的临床试验未纳入足够数量的65岁及以上患者,无法确定他们的反应是否与年轻患者不同。
【药物相互作用】
CYP3A4抑制剂
应避免将强效和中效CYP3A4抑制剂与Dordaviprone同时使用。对于成人和体重至少52.5kg的儿科患者,若无法避免同时使用,应按推荐减少Dordaviprone的剂量。
CYP3A4诱导剂
应避免将强效和中效CYP3A4诱导剂与Dordaviprone同时使用。
已知可延长QTc间期的药物
应避免将Dordaviprone与已知可延长QTc间期的产品同时使用。若无法避免同时使用,应将Dordaviprone与该延长QT间期的产品分开给药。
【药物过量】
尚不明确。如有发生药物过量请及时就医,对症治疗。
【药代动力学】
在获批推荐剂量下,单次给药后Dordaviprone在患者体内的药代动力学参数已被预测,除非另有说明,否则均以平均值(变异系数%)呈现。Dordaviprone的血药峰浓度(Cmax)为2.8微克/毫升(42%),总全身暴露量(AUC)为23小时・微克/毫升(48%)。在125至625毫克的剂量范围内,Dordaviprone的Cmax和AUC随剂量成比例增加。每周一次给药后未观察到药物蓄积现象。
吸收
Dordaviprone达到血药峰浓度的中位时间(Tmax)(最小值,最大值)为1.4小时(0.5,5.6小时)。
食物影响
与高脂餐(800至1000卡路里,50%脂肪)同服时,Dordaviprone的Cmax下降40%,而AUC无变化。
分布
Dordaviprone的表观(口服)分布容积为450升(40%)。
体外研究显示,Dordaviprone的血浆蛋白结合率为95%至97%,且与浓度无关。
体外研究中,血药与血浆浓度的中位比值为0.67。
代谢
Dordaviprone主要经CYP3A4代谢,CYP2B6、CYP2C8、CYP2C9、CYP2D6和CYP3A5也有少量参与。
排泄
Dordaviprone的平均终末半衰期为11小时(30%),表观清除率约为27升/小时(48%)。
单次给予放射性标记的Dordaviprone后,70%的剂量在尿液中回收,20%在粪便中回收,且尿液和粪便中均未检测到明显的未代谢Dordaviprone。
多达维普龙的获批为H3 K27M突变型弥漫性中线胶质瘤的治疗带来了新的契机。未来,随着对该药物研究的深入,有望进一步优化治疗方案,提高治疗效果。请咨询康必行海外医疗医学顾问:4006-130-650或扫码添加下方微信,我们将竭诚为您服务!
更多药品详情请访问 多达维普龙 https://www.kangbixing.com/drug/ddwpl/




 添加康必行顾问,想问就问
添加康必行顾问,想问就问