
继2017年8月美国批准第一款用于治疗儿童白血病 CAR-T 产品后,FDA于2017年10月18日再次批准Kite制药公司(Kite Pharma)第二款CAR-T细胞疗法――Axicabtagene ciloleucel (商品名: Yescarta )的销售, Yescarta可用于既往接受二线或多线系统治疗的复发...

2017年8月30日, CAR-T 技术迎来了其发展历程中的历史性时刻。美国FDA已经批准诺华公司的突破性CAR-T疗法Kymriah(tisagenlecleucel,CTL019),治疗罹患B细胞前体急性淋巴性白血病(ALL),且病情难治,或出现二次及以上复发的25岁以下患者。值得一提的是,...
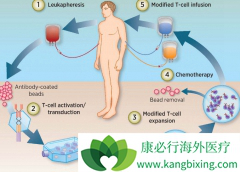
诺华公司授权该技术,并且可以大规模制造 Kymriah 细胞,计划到年底在美国约有30家医院开设car-t治疗。 CAR-T是一种高度个性化的方法,每个人的细胞和接受过的治疗都不同,如同Emily一样,许多患者在接受 CAR-T 治疗前已经接受过各种治疗方法,如骨髓移...
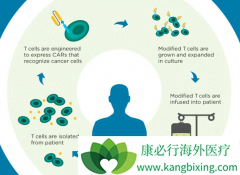
CAR-T 细胞治疗从内部开始治疗,通过增强身体自身免疫系统与基因增强来对抗癌症。来自纪念斯隆凯特琳癌症中心的小儿骨髓移植服务的凯文・柯兰博士说:“这是一个典型的转变。 “这些治疗实际上是利用我们系统的活细胞,在实验室中修改,教导它们如何找...
FDA官方宣布批准诺华公司的突破性 CAR-T 新药CTL019(商品名Kymriah)正式上市,用于治疗B细胞前体急性淋巴性白血病(ALL),且病情难治,或出现两次及以上复发的25岁以下患者。这是美国批准的第一个基因疗法。 因为 CAR-T 可能诱发细胞因子风暴(CRS)...
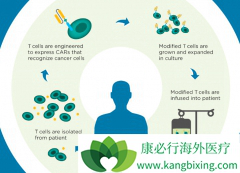
2017年,诺华和吉利德的两款 CAR-T 细胞产品获批上市,书写了CAR-T细胞疗法时代的开卷语。T细胞受体(T cell receptor,TCR)疗法和嵌合抗原受体(chimeric antigen receptor,CAR)T细胞疗法都是利用患者自身的T淋巴细胞治疗癌症的两类前沿基因疗法。...
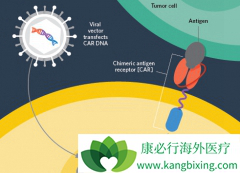
在今年2月23号,Gilead旗下公司Kite与Sangamo Therapeutics达成全球合作,使用Sangamo的锌指核酸酶ZNFs技术平台开发下一代肿瘤学离体 细胞治疗 。根据协议的条款,Sangamo将获得1.5亿美元的预付款,并有资格获得高达30.1亿美元的潜在付款。 这...

近日,CAR-T疗法连续取得突破性成果!先是,来自美国和意大利的科学家团队为CAR-T对抗一种致命脑瘤找到了更好的靶点;紧接着,来自日本的研究小组开发了一种升级版的CAR-T疗法,可使得小鼠实体瘤完全消除。 2月28日,发表在Science Translation...
Kymriah 和Yescarta一次治疗的费用分别是47.5万和37.3万美元,而Luxturna更是预测将达到100万美元!为何这些治疗费用如此高昂,真的会有人为此买单吗,这到底是制药公司的恶意垄断,还是背后另有原因? 药品是特殊的商品。凡是商品就会有自己...

8月30日,FDA正式批准诺华 CAR-T 疗法 Kymriah(tisagenlecleucel,CTL-019)上市,用于治疗儿童和年轻成人(2~25岁)的急性淋巴细胞白血病(ALL),FDA的这一决定比预定的审批期限提前了1个月。 Kymriah被FDA明确定性为以细胞工程为基础的基因...
免费咨询电话:4006 130 650


