2021年5月27日,Myovant Sciences公司和辉瑞(Pfizer)宣布,美国FDA已批准 瑞卢戈利 (瑞卢戈利 40 mg、雌二醇1 mg和醋酸炔诺酮0.5 mg)上市。新闻稿指出,这是首个每日一次,治疗绝经前女性子宫肌瘤相关月经大量出血的药物,治疗持续时间可长达24个月。此 ...
第一三共(Daiichi Sankyo)和阿斯利康(AstraZeneca)公司共同开发的靶向HER2的抗体偶联药物(ADC) Enhertu (fam-trastuzumab deruxtecan-nxki,DS-8201),在治疗先前接受过治疗的HER2过度表达癌症患者的1期临床试验中,将55.6%的非小细胞肺癌(NSCLC)患 ...
艾伯维(AbbVie)和基因泰克(Genentech)公司宣布,双方联合开发的 维奈克拉 (venetoclax)与低甲基化剂azacitidine联合,在治疗急性髓系白血病(AML)患者的3期临床试验VIALE-A(M15-656)中,达到了双重主要临床终点。该组合疗法与azacitidine和安慰剂构 ...
2020年10月16日,美国食品药品监督管理局(FDA)批准将阿扎胞苷(维达莎)与 维奈克拉 联合用于≥75岁或患有合并症而不能进行强化诱导化疗的新诊断的急性髓系白血病(AML)患者。 本次美国FDA批准阿扎胞苷联合维奈克拉的新适应症是基于VIALE-A研究的显著 ...
在妊娠、老年人、儿童、肝功能严重损害等特殊人群中如何应用 TAF ?过去,关于药物的妊娠安全性,大家一直沿用ABCDX的分级标准,简单来说,X类药物为妊娠和计划妊娠妇女禁用(例如干扰素),而A类和B类药物可以用于妊娠妇女。在口服NA中,TAF和TDF均为B类药 ...

慢性乙型肝炎长期抗病毒治疗中的药物安全是临床关注的首要问题。刚刚在我国获批的富马酸丙酚替诺福韦( TAF )的一大优势就是靶向肝脏,从而大幅改善了对肾脏和骨骼的安全性,进一步增加了长期用药的安全系数。不过药物安全并不只需要考虑肾脏,TAF的其他安 ...
在美国, 丙通沙 于2020年3月获得FDA批准,用于治疗年龄≥6岁、体重≥17公斤的慢性丙型肝炎儿科患者(无论HCV基因型或肝病严重程度如何)。用药方面,丙通沙在≥6岁儿童中的推荐剂量基于体重和肝功能。值得一提的是,丙通沙是获批用于治疗丙肝成人患者和儿童 ...
丙通沙 是首个全口服、泛基因型、每日一次单片方案(STR),于2016年6月28日获得FDA批准,用于无肝硬化或伴有代偿期肝硬化的全部6种基因型(GT 1-6)丙肝成人患者,以及联合利巴韦林(RBV)用于伴有失代偿期肝硬化的丙肝成人患者。2017年,美国食品和药物管 ...
家族性地中海热(FMF)是较常见的遗传性单基因自身炎症性疾病。它是由MEFV基因功能缺失突变引起的,主要影响东地中海地区的人群。秋水仙碱是治疗FMF的主要方法,可预防急性发作和淀粉样变性,减少慢性炎症。对于秋水仙碱耐药或不耐受患者,对FMF发病机理的最 ...
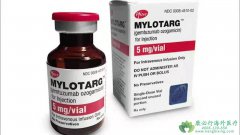
2017年9月1日美国食品和药品监管局今天批准 吉妥珠单抗 (gemtuzumab ozogamicin)适用于新诊断出肿瘤表达CD33抗原阳性的急性髓性白血病成年的治疗患者,(CD33-阳性AML)。FDA还批准吉妥珠单抗对年龄2岁和以上有CD33-阳性并且既往经历过复发或对初始治疗无效( ...
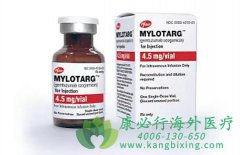
Mylotarg 是一种实验性抗体药物偶联物(ADC),由细胞毒性制剂卡奇霉素(calicheamicin)和靶向CD33的一种单克隆抗体偶联而成。CD33是一种抗原蛋白,表达于超过90%的AML患者的成髓细胞(myeloblast)的表面。当Mylotarg结合至细胞表面的CD33抗原时被吸收进入 ...

Horizon治疗公司于近日公布了2项临床试验的阳性数据,这些数据为 TEPEZZA (teprotumumab-trbw)治疗甲状腺眼病(ThyroidEyeDisease,TED)的有效性和安全性提供了更多的证据。TEPEZZA是首个且是唯一经美国FDA批准的TED治疗药物。TED是一种严重的、进行性的、 ...
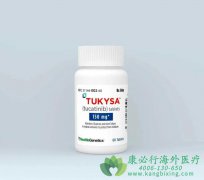
乳腺癌中大约有20%~25的类型为HER2阳性,该类型中有34%的患者会发生脑转移。目前HER2阳性晚期乳腺癌标准治疗的一线用药为曲妥珠单抗和帕妥珠单抗联合紫杉类化学疗法,二线治疗为T-DM1,但病情发生再次进展后该如何治疗,目前没有统一的标准方案。对于发生脑 ...
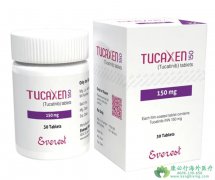
2020年4月17日,美国FDA批准HER2特异性抑制剂 图卡替尼 (Tucatinib)与曲妥珠单抗和卡培他滨联用,用于治疗手术无法切除或转移性经治的晚期HER2阳性乳腺癌患者。 图卡替尼的批准是基于HER2CLIMB临床试验的数据。HER2CLIMB是一项随机、双盲、安慰剂对照 ...

2021年05月29日,美国食品和药物管理局(FDA)已批准靶向抗癌药 索托拉西布 (sotorasib,AMG 510),该药是一种KRASG12C抑制剂,用于治疗先前已接受过至少一种系统疗法、经FDA批准的检测方法证实存在KRAS G12C突变、局部晚期或转移性非小细胞肺癌(NSCLC)成 ...
根据2021年世界肺癌大会期间公布的正在进行的1/2期CodeBreaK 100试验(NCT03600883)的后期分析数据,对KRAS G12C突变型非小细胞肺癌(NSCLC)和稳定性脑转移患者(既往接受过放疗或手术),使用 索托拉西布 (Lumakras,AMG510,索托拉西布)治疗后,观察到强大的 ...

2021年世界肺癌会议发布的数据显示,对于既往接受过治疗的携带EGFR 20号外显子插入突变的非小细胞肺癌(NSCLC)患者,用 mobocertinib (原名TAK-788)治疗显示出患者报告结果(PROs)的改善。西班牙阿科鲁尼亚大学医院的Maria Rosario Garcia Campelo博士表 ...
非小细胞肺癌是最常见的肺癌,EGFR外显子20插入突变的患者约占非小细胞肺癌患者的1-2%,预后较差。对EGFR-TKI(表皮生长因子受体络氨酸激酶抑制剂)治疗有效的患者最终都会产生耐药性。因此,该类患者亟需新的治疗方案。 根据国际肺癌研究协会(IASLC) 20 ...

2021年5月21日,美国食品药品监督管理局(FDA)加速批准强生公司研发生产的EGFR/c-Met双抗 Rybrevant 上市,用于治疗铂类化疗后进展的EGFR外显子20插入突变(EGFR20ins)的转移性非小细胞肺癌(NSCLC)患者。这是FDA批准的首个针对该类突变的药物。EGFR外显 ...

美国时间2021年5月21日,强生旗下的杨森制药公司宣布,美国FDA加速批准了该公司研发的EGFR/MET双特异性抗体疗法 Rybrevant (amivantamab-vmjw)上市,用于治疗经FDA批准的测试确认的患有表皮生长因子受体(EGFR)外显子20插入突变的局部晚期或转移性非小细 ...

扫一扫康必行专业医学顾问免费咨询
免费咨询电话:4006 130 650

